Stamceltherapie voor verwondingen aan de pezen van paarden
SDFT-verwondingen bij paarden en regeneratieve geneeskunde
Oppervlakkige verwondingen van de digitale flexorpees (SDFT) zijn een belangrijke oorzaak van kreupelheid en verminderd atletisch vermogen binnen de paarden atletische industrie, met een beschreven prevalentie van 8 tot 43% bij volbloed renpaarden (Dowling, 2000). Dit komt door de hoge prevalentie van deze verwondingen, de verlengde herstelperiode en het hoge percentage recidieven. SDFT-blessures genezen langzaam, met 20-60% van de gewonde racepaarden die weer volledig atletisch worden, maar waarbij tot 80% van de gewonde racepaarden bezwijkt aan opnieuw letsel (Dowling, 2000). Deze neiging om langzaam te genezen, en de constructie van mechanisch kleinere extracellulaire matrix, is waarschijnlijk te wijten aan het feit dat pezen minimaal gevasculariseerd zijn, cellen met verminderde mitotische werking hebben en weinig progenitorcellen in de weefsels hebben. Recent onderzoek naar mesenchymale stamcellen (MSC's) impliceerde de mogelijke ontwikkeling van het gebruik van regeneratieve medicijnen als een mogelijke nieuwe behandeling voor SDFT-letsels.
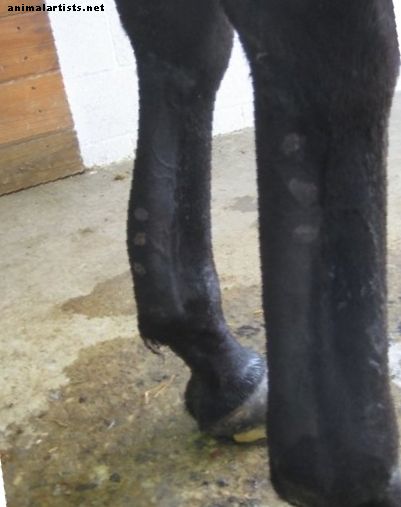
Oppervlakkige verwondingen van de digitale flexorpees (SDFT) zijn een belangrijke oorzaak van kreupelheid en verminderd atletisch vermogen binnen de paarden atletische industrie, met een beschreven prevalentie van 8 tot 43% bij volbloed renpaarden.
Peesstructuur bij een paard
Pezen bestaan voor het grootste deel uit water (~ 70%); de resterende 30% bevat collageen en een collageenvrije matrix. Binnen normale flexorpezen komt type I collageen het meest voor. Type II, III, IV en V bestaan ook, hoewel in mindere hoeveelheden in meer specifieke posities binnen de pees. Type II kan worden geplaatst in benige invoegingen en gebieden waar de pees van richting verandert om een benige projectie te bedekken, en is ontworpen om compressie en spanning te weerstaan. Type III, IV en V komen alleen voor in basale membranen en endotendon. Collageenmoleculen zijn georganiseerd in microfibrillen, subfibrillen en fibrillen en worden verder gecategoriseerd in fascikels die losjes worden gescheiden door endotenon-septa, en de resterende matrix bestaat uit tenocyten en glycoproteïnen. Celtypen I, II en III zijn herkend in de fascikels van paardenpezen. De toewijzing van deze cellen verschilt met de leeftijd en kan meestal worden geassocieerd met extracellulaire matrixsynthese. Verschillende glycosaminoglycanen zijn gevonden in normale SDFT's, waaronder chondroïtinesulfaat, kerataansulfaat, dermatansulfaat, heparine, heparinsulfaat en hyaluronzuur. Proteoglycansdecorin, fibromoduline en biglycan komen overal in de SDFT voor en beïnvloeden tenocytfuncties, collageenfibrillogenese en dimensionale rangschikking van vezels. Dit beïnvloedt de sterkte van de pees. Proteoglycanen spelen mogelijk ook een rol bij het in beslag nemen van groeifactoren in de collageenmatrix.
Pezen bestaan voor het grootste deel uit water (~ 70%); de resterende 30% bevat collageen en een collageenvrije matrix.
Gemeenschappelijke peesblessures van het paard
In de natuur voorkomende peesblessures worden beschreven als "uitrekken, slippen en scheuren van de fibrillair, gevolgd door fibrilolyse" die is gekoppeld aan de "afgifte van enzymen uit beschadigde fibroblasten en ontstekingscellen" (Dowling, 2000). Het is daar dat het genezingsproces begint, gevolgd door overliggende fasen van ontsteking, proliferatie, hermodellering en rijping. Type III collageen is het eerste dat op de plaats van de verwonding wordt geïntegreerd en de interibrillaire dwarsverbindingen vormt die zorgen voor vroege sterkte en stabiliteit op de plaats van verwonding. Verhoogde hoeveelheden type IV en type V collageen ontwikkelen zich dan snel. Na deze acute fasen worden type I collageenvezels het duidelijkst zichtbaar en verschijnen vrije type I en type III collageenfibrillen in enigszins kleinere hoeveelheden tot ongeveer 6 maanden na verwonding. Vervolgens overheersen type I collageenfibrillen opnieuw, wat indicatief is voor de continue hermodellering en normalisatie van het genezende weefsel. Abnormaal hoge niveaus van type III collageen en afwezigheid van een rechtlijnig samenstel kunnen aanwezig zijn tot veertien maanden na letsel. In vezelachtig littekenweefsel wordt gedacht dat de abnormale rangschikking en samenstelling van matrix, die zelfs slechtere biomechanica heeft in vergelijking met gemiddeld peesweefsel, en de verminderde genezingssnelheid de oorzaak zijn van de verhoogde snelheid van opnieuw letsel aan de SDFT. Voor meer informatie over paardenpezen en gewone peesblessures (behalve knieblessures) raad ik aan te verwijzen naar Howell Equine Handbook of Pees- en ligamentverwondingen.
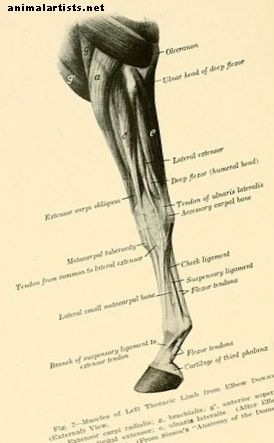
In de natuur voorkomende peesblessures worden beschreven als "uitrekken, slippen en scheuren van de fibrillair, gevolgd door fibrilolyse" die is gekoppeld aan de "afgifte van enzymen uit beschadigde fibroblasten en ontstekingscellen."
Huidige therapie-opties in paardengeneeskunde
Er zijn verschillende momenteel geaccepteerde opties beschikbaar voor het behandelen van SDFT-letsels. Deze therapieopties kunnen worden onderverdeeld in fysieke, farmacologische, chirurgische therapieën. Fysieke therapieën bestaan in de vorm van ijsvorming, koude hydrotherapie, drukverband en kraamrust en worden beschouwd als de hoeksteen in de beginfase van een SDFT-letselbehandeling om ontstekingen te verminderen en de kans op verdere schade te verminderen. Fysieke therapieën worden vaak gebruikt in combinatie met medicamenteuze therapieën. Medicamenteuze regimes omvatten gewoonlijk ontstekingsremmers, natriumhyaluronaat, polysulfaatglycosaminoglycanen en beta-aminoproprionitrilfumaraat. Corrigerende chirurgische opties omvatten momenteel accessoire ligament desmotomie, percutane pezen splitsen, synthetische peesimplantaten en contrairritatie. Andere, minder bestudeerde therapie-opties zijn onder andere therapeutische lage intensiteit ultrasound, lage frequentie infrarood lasertherapie en elektromagnetische veldtherapie. De resultaten van dergelijke behandelingen zijn gevarieerd, omdat er minimale aantoonbare gegevens zijn dat een van de bovengenoemde therapieopties consequent betrouwbare of langdurige voordelen heeft gehad. Dit is waarschijnlijk gedeeltelijk te wijten aan de grote variatie in therapietechnieken en voorkeuren bij dierenartsen en eigenaren.
Fysieke therapieën bestaan in de vorm van ijsvorming, koude hydrotherapie, drukverband en kraamrust en worden beschouwd als de hoeksteen in de beginfase van een SDFT-letselbehandeling om ontstekingen te verminderen en de kans op verdere schade te verminderen.
Mesenchymale stamcel (MSC) therapie in paardengeneeskunde
Mesenchymale stamcellen zijn niet-hematopoietische multiponentstamcellen die van belang zijn voor gebruik bij de therapie van orthopedische verwondingen bij paarden. Stamcellen worden gecategoriseerd als embryonale of volwassen cellen, afhankelijk van het ontwikkelingsniveau van hun donor. Voor het doel van deze studie zal de nadruk hier liggen op volwassen cellen. Volwassen stamcellen zijn een normaal verblijvende populatie cellen die in elk weefseltype worden gevonden en helpen om de juiste orgaanvorm te bieden tijdens reguliere cellulaire omzetprocessen. Deze stamcellen kunnen ook naar behoefte differentiëren naar andere celtypen van verschillende weefseloorsprong, wat celplasticiteit wordt genoemd. Het gebruik van MSC's voor weefselregeneratie werd eerst gepromoot op basis van dit idee van celplasticiteit; beschadigde weefsels zouden direct worden gestimuleerd door de injectie van MSC's, de cellen bevolken de plaats van verwonding, differentiëren in het juiste celtype voor dat weefsel en de regeneratie zou beginnen. Later werd gevonden dat deze cellen ook regeneratie indirect zouden stimuleren door bioactieve trofische en immunomodulerende factoren te produceren.
Vetweefsel en beenmerg zijn de twee meest gebruikelijke bronnen van MSC's die worden gebruikt voor paardengeneeskunde, hoewel bronnen zoals perifeer bloed en navelstrengbloed aan populariteit winnen, omdat ze minder invasief zijn. In vergelijking met menselijke MSC's zijn er momenteel geen karakterisatienormen beschikbaar voor MSC's van dierlijke oorsprong. Daarom gebruiken verschillende bedrijven verschillende methoden om MSC's van dieren te karakteriseren, waardoor het moeilijk is om onderzoeksresultaten en klinische resultaten van MSC-therapieën die bij paarden worden gebruikt, te vergelijken. Hoewel MSC's van dieren kunnen worden geclassificeerd op basis van hun vermogen om zich aan plastic te hechten en te differentiëren, is hun oppervlakte-antigeenexpressie nog steeds niet gemakkelijk te identificeren. Deze beperkte beschikbaarheid van specifieke antilichamen in de diergeneeskunde beperkt de mogelijkheden van echte immunofenotypering van MSC's.
Resultaten van huidige MSC-studies
In 2003 werd het gebruik van MSC's voor gebruik als therapie voor verwondingen van paardenpezen voor het eerst gedefinieerd, met slechts vijf onderzoeksartikelen over het onderwerp gepubliceerd (Van de Walle, 2016). Na die gebeurtenis is het gebruik van MSC's in de regeneratieve geneeskunde voor paarden enorm gestegen, waarbij duizenden paarden nu met deze methode worden behandeld. De werkzaamheid van MSC-therapieën bij paarden is echter nog steeds enigszins onzeker, omdat geschikte controlegroepen niet altijd worden gebruikt en andere biologische factoren vaak worden gebruikt in combinatie met stamcellen. Toch heeft eerder onderzoek een positief verband aangetoond tussen mesenchymale stamceltherapie en gezonde peesregeneratie bij SDFT-letsels, met enkele aantoonbare verlaagde percentages van opnieuw letsel (Badial, 2013; Carvalho, 2011; Godwin, 2013; Guercio, 2015; Smith, 2003).
Een studie uit 2013 gebruikte met name vergelijkbare methoden als deze studie. In deze vorige studie werden laesies geïnduceerd met behulp van een collagenase-gelinjectie in het middenrifgebied van de SDFT's van acht paarden van gemengde rassen. Paarden in de behandelingsgroep werden behandeld met een interlesionale injectie van mesenchymale stamcellen afgeleid van vetweefsel gesuspendeerd in bloedplaatjesconcentraat. Na 16 weken behandeling werden biopten uitgevoerd voor histopathologische, immunohistochemische en genexpressieanalyses. De resultaten van deze studie toonden aan dat het gebruik van mesenchymale stamcellen en bloedplaatjesconcentraat de progressie van peesletsels voorkwam, resulteerde in een superieure celrangschikking en verminderde ontsteking in vergelijking met de controlegroep. (Badial, 2013)
Een onderzoek uit 2014 van negen paarden met reeds bestaand SDFT-letsel merkte bewijs op van reparatieve weefselprocessen na de behandeling na gebruik van van vet afgeleide mesenchymale stamcellen als behandelingsmethode (Guercio, 2014). Een tweejarig onderzoek uit 2012 van 141 client-eigendom renpaarden met reeds bestaande verwondingen gebruikte stamcellen afgeleid van beenmerg in plaats van vetcellen, maar constateerde geen nadelige effecten van de behandeling; er werd echter een significante daling van het aantal blessures bij renpaarden waargenomen (Godwin, 2012).
Hoewel deze eerdere studies allemaal hebben geprobeerd een verband tussen SDFT-verwondingen en mesenchymale stamcellen waar te nemen, zijn er veel verwarrende factoren en veel voor de hand liggende hiaten in dit onderzoek. Sommige studies hebben onvoldoende gebruik gemaakt van onderwerpen om overtuigend bewijs te leveren, anderen gebruikten een breed scala aan rassen, leeftijden, geslachten en atletische disciplines. Anderen gebruiken een wisselend aantal stamcellen en behandelingsintervallen. Misschien is de grootste verstorende factor dat de meeste van deze onderzoeken paarden met reeds bestaand letsel gebruikten, waardoor een grote variatie in letselgrootte, ernst, duur, enz. Ontstond en niet kon bepalen of deze factoren een verband hadden met de resultaten. Door een grotere groep paarden met leeftijd, geslacht, ras en discipline te gebruiken, een vooraf ingesteld aantal stamcellen, een specifiek letsel, behandelplan en behandelingsinterval, en door te streven naar relaties tussen deze factoren en de resultaten, nieuwe studies moeten ernaar streven om confounding factoren te verminderen en meer overtuigend bewijs te verkrijgen. Vanaf dat moment is aanvullend onderzoek nodig om de effecten van stamceltherapie bij paarden te onderzoeken.
SDFT-blessures en MSC's Quiz
quizstatistieken bekijkenReferenties
Badial, P., Deffune, E., Borges, A., Carvalho, A., Yamada, A., Álvarez, L., Garcia Alves, A. (2013). Peesontsteking bij paarden met mesenchymale stamcellen en bloedplaatjesconcentraten: een gerandomiseerde, gecontroleerde studie. Stamcelonderzoek en therapie, 4 (4), 1-13. doi: 10, 1186 / scrt236
Crovace, A., Lacitignola, L., Rossi, G., Francioso, E. (2009). Histologische en immunohistochemische evaluatie van autologe gekweekte mesenchymale stamcellen en beenmergmononucleaire cellen in door collagenase geïnduceerde tendinitis van oppervlakkige digitale flexorenpees bij paarden. Veterinary Medicine International, 2010, 1-10. doi: 10, 4061 / 2010/25097
Dowling, BA, Dart, AJ, Hodgson, DR en Smith, RKW (2000), oppervlakkige digitale flexor tendinitis bij het paard. Equine Veterinary Journal, 32: 369–378. doi: 10, 2746 / 042516400777591138
Godwin, EE, Young, NJ, Dudhia, J., Beamish, IC en Smith, RKW (2012). Implantatie van uit beenmerg afgeleide mesenchymale stamcellen toont verbeterde uitkomst bij paarden met overbelastingsletsel van de oppervlakkige digitale flexorpees. Equine Veterinary Journal, 44 (1): 25–32. doi: 10.1111 / j.2042-3306.2011.00363.x
Guercio, A., Di Marco, P., Casella, S., Russotto, L., Puglisi, F., Majolino, C., Piccione, G. (2015). Mesenchymale stamcellen afgeleid van onderhuids vet en bloedplaatjesrijk plasma dat wordt gebruikt bij atletische paarden met kreupelheid van de oppervlakkige digitale flexorpees. Journal Of Equine Veterinary Science, 35 (1), 19-26. doi: 10.1016 / j.jevs.2014.10.006
Richardson LE, Dudhia J., Clegg PD, Smith, R. (2007). Stamcellen in de diergeneeskunde - pogingen om paardenpees na verwonding te regenereren. Trends in Biotechnology, 25 (9), 409-16.
Van de Walle, G., De Schauwer, C., Fortier, L. (2016). Mesenchymale stamceltherapie. Equine Clinical Immunology (1 e ed.) John Wiley & Sons, Inc.